ERFAHRUNG AUS 105 NEUROCHIRURGISCHEN EINGRIFFEN MIT INTRAOPERATIVEM ELEKTROPHYSIOLOGISCHEN MONITORING
Experiences in Intra-operative Electrophysiological Monitoring of 105 Neurosurgical Procedures
Aus der Abteilung Neurochirurgie (Leitender Arzt: Oberstarzt Prof. Dr. U. Kunz) am Bundeswehrkrankenhaus Ulm (Chefarzt: Generalarzt Prof. Dr. Dr. E. Grunwald)
Eduard Stettin, Andrea Schwanbeck, Chris Schulz, Ulrich Kunz, Frank Weber und Uwe Max Mauer
Die Überwachung neurologischer Funktionen während einer Operation mittels elektrophysiologischer Methoden findet eine zunehmende Verbreitung.
Methoden:
In 105 neurochirurgischen Eingriffen wurde intraoperatives elektrophysiologisches Monitoring (IOM) in der Abteilung Neurochirurgie am Bundeswehrkrankenhaus Ulm angewendet.
Ergebnisse:
Durch das IOM konnten 14 richtig positive, postoperativ beobachtete, neurologische Störungen korrekt vorhergesagt werden. Bei 58 Eingriffen wurde durch das IOM eine Potenzialveränderung angezeigt.
Schlussfolgerungen:
Die hieraus resultierende Änderung der operativen Strategie hat wahrscheinlich eine Verschlechterung des präoperativen neurologischen Status verhindert. In den übrigen Fällen wurde intraoperativ keine Verschlechterung der Potenziale detektiert und der neurologische Status war nach der Operation unverändert. Ein falsch negatives Ergebnis trat bei keinem Eingriff auf.
Summary
Background:
Intra-operative neuromonitoring is becoming a valuable part of surgical procedures. Methods: We used intra-operative electrophysiological monitoring (IOM) in 105 neurosurgical procedures.
Results:
Because of IOM 14 true positive neurological deficits were predictable. In 58 procedures it was probably possible to prevent worsening of preoperative neurological status. A false negative result did not occur.
Conclusions:
The correct application of intraoperative neuromonitoring leads to improved surgical outcome. Keywords: neurosurgery, intra-operative monitoring, evoked potentials
1. Einführung
Mit Hilfe von elektrischer Stimulation kann die Funktionalität von Nervenbahnen im zentralen Nervensystem dargestellt und deshalb bei Eingriffen am Nervensystem überwacht werden. Mit der Entwicklung neuer Ableitungsmöglichkeiten wie beispielsweise der transkraniellen elektrischen Stimulation für MEP (motorisch evozierte Potenziale) oder DWellen ist seit einigen Jahren eine genauere Überwachung der motorischen Funktionen während der operativen Eingriffe möglich geworden (Tab 1).
Kommt es zu Veränderungen in den Ableitungen, bedeutet dies eine Einschränkung der neurologischen Funktion des überwachten Areals. Bei sensibel (SEP), motorisch (MEP) oder akustisch (AEP) evozierten Potenzialen können die Amplituden der Potenziale verkleinert oder die Latenzzeiten verlängert sein. Diese Veränderungen sind zumeist reversibel, sodass eine drohende Schädigung angezeigt werden kann. Erfolgt dann eine Änderung im Operationsablauf, kann eine permanente Schädigung vermieden werden. Häufig sind behebbare Ursachen für eine Änderung des Potenzials auszumachen. So können durch ein anderes Platzieren des Spatels und der Watteabdeckung, eine vorsichtigere Präparation, eine Präparationspause oder einen zurückhaltenden Einsatz der bipolaren Koagulation in empfindlichen Arealen die Potenziale bereits wieder verbessert werden.
2. Methoden
Operationsspektrum
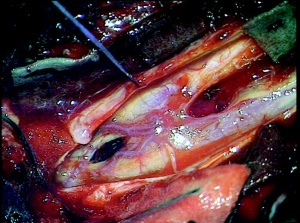
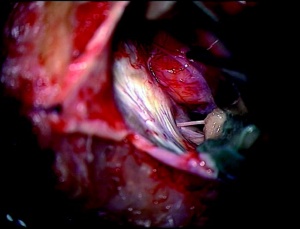
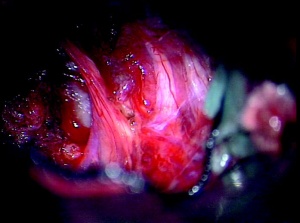
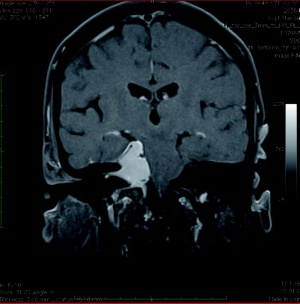
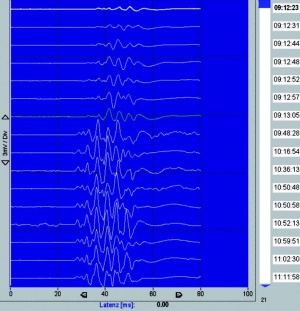
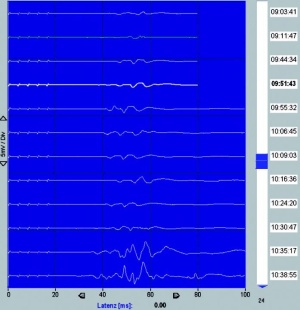
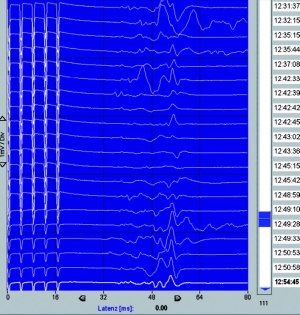
Seit 2007 wurden in der Neurochirurgie am Bundeswehrkrankenhaus (BwKrhs) Ulm insgesamt 105 Operationen mit intraoperativem elektrophysiologischem Monitoring (IOM) durchgeführt. Davon waren 44 Eingriffe bei intraspinalen Raumforderungen (Abb 1), 13 Eingriffe im Kleinhirnbrückenwinkel (Abb 2 links, 2 rechts, 3 oben, 3 unten), 9 Eingriffe bei mikrovaskulären Dekompressionen am Hirnstamm, 10 Eingriffe an peripheren Nerventumoren oder Verletzungen. Weitere Eingriffe mit IOM erfolgten unter anderem bei Aneurysmaclipping, Gliomresektion und Tethered Cord Release.
Nervenstimulationsmethoden
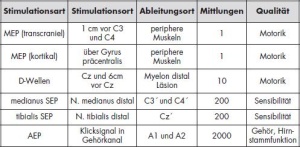
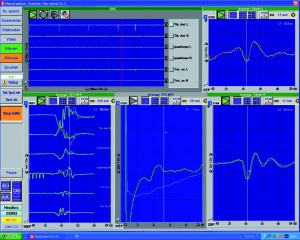
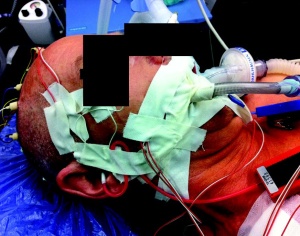
Abgeleitet wurden transkraniell elektrische oder direkt kortikale MEP, D-Wellen, Medianus- und Tibialis-SEP, AEP, Phasenumkehr, EMG (Elektromyographie) und direkte Nervenstimulationen (Tab 2). Verwendet wurde das Gerät ISIS IOM der Firma Inomed (Abb 4). Die Darstellung der verschiedenen Ableitungen erfolgte über die hierfür eigens entwickelte Software „Neuroexplorer“. VEP (visuell evozierte Potenziale) werden bis jetzt in unserer Abteilung nicht abgeleitet. Es gibt Studien die zeigen, dass die Aussagekraft von VEP-Änderungen für eine iatrogene Schädigung intraoperativ eingeschränkt ist [1].
MEP dienen in unserer Abteilung dazu, die motorischen Funktionen bei Eingriffen am zentralen Nervensystem zu überwachen. Die Stimulation erfolgte entweder transkraniell elektrisch (5 Pulse mit 150 mA und einer Pulsbreite von 0,3 - 0,5 ms) über den Punkten 1 cm vor C3 und 1 cm vor C4 entsprechend des internationalen 10/20-Systems (Abb 5) oder direkt kortikal mit einer Streifenelektrode oberhalb des motorischen Kortexareals (5 Pulse mit maximal 30 mA und einer Pulsbreite von 0,3 - 0,5 ms). Das Bewegungsartefakt fällt bei direkter kortikaler Stimulation schwächer aus, weil eine selektivere Stimulation des motorischen Kortexareals möglich ist.
Die periphere Stimulation bei SEP wurde mit Nadelelektroden mit 10 – 30 mA bis zur motorischen Antwort des stimulierten Nerven durchgeführt. Die Ableitung erfolgte über Cz, C3 und C4 entsprechend des internationalen 10/20-Systems. Es wurden 200 Mittlungen ausgewertet.
Die Klicksignale der AEP wurden mittels eines in den Gehörgang eingeführten Stöpsels weitergeleitet. Die maximale Lautstärke betrug 90 dB bei 1 000 - 2 000 Mittlungen. Anstelle des üblichen Ableitungsortes oberhalb des Mastoids wurde zumeist vor dem Tragus des ipsilateralen Ohres, bedingt durch den für den operativen Zugang benötigten retromastoidalen Zugangsweg, abgeleitet.
Eine weitere Überwachungsmöglichkeit der spinalen motorischen Aktivität ist die Ableitung von D-Wellen. Hierfür wird ein Katheter direkt in den spinalen Epiduralraum unterhalb der operierten Höhe eingeführt. Der D-Wellenkatheter muss hierfür oberhalb des Myelons eingebracht werden, eine D-Wellen-Ableitung oberhalb der Cauda equina ist nicht möglich. Die D-Wellenkatheter werden dazu gewöhnlich vom OP-Gebiet aus nach distal der Läsion in den Epiduralraum eingebracht. Die außerdem mögliche perkutane Applikation, ähnlich wie bei der Anlage eines epiduralen Katheters zur Schmerztherapie, wurde nicht gewählt. Als Stimulationsparameter diente ein Puls mit 40 – 150 mA oberhalb von Cz und 6 cm vor Cz in der Mittellinie entsprechend des internationalen 10/20-Systems. Kommt es hierbei zu Veränderungen in den abgeleiteten Kurven, wird der Operateur entweder akustisch durch ein Analysesystem des Monitoringgerätes oder durch den jeweiligen Benutzer mündlich informiert. Hieraus kann sich dann eine Änderung im aktuellen Operationsablauf ergeben.
EMG-Ableitungen werden zur Überwachung motorischer Hirnnervenfunktionen, bei spinalen Operationen zur Überwachung von bestimmten Spinalwurzeln oder bei Eingriffen an peripheren Nerven, die motorische Fasern enthalten, angewendet. Durch die auftretenden Potenziale (burst, train) kann eine Irritation des Nerven angezeigt werden. Bei vermehrtem Auftreten von „trains“ ist eine axonale Schädigung des Nerven beziehungsweise der Nervenwurzel wahrscheinlich. Zur Regenerationswahrscheinlichkeit oder Schwere der Schädigung lässt sich mittels EMG nur eine bedingte Aussage treffen.
Anästhesie
Alle Eingriffe wurden in Intubationsnarkose durchgeführt. Bei allen Patienten wurde eine TIVA (totalintravenöse Anästhesie) verwendet. Da bei der überwiegenden Anzahl der Patienten auch eine EMG-Ableitung erfolgte, wurden die Eingriffe ohne Relaxierung durchgeführt. Insbesondere bei spinalen Eingriffen mit transkranieller elektrischer Stimulation kommt es daher durch das Auslösen eines MEP zu einem deutlichen Bewegungsartefakt. Bei der Durchführung muss darauf geachtet werden, dass sich keine Instrumente im operativen Situs befinden. Bei direkter kortikaler Stimulation fallen die Bewegungsartefakte deutlich schwächer aus.
Alle Patienten wurden im Rahmen der Operationsaufklärung über die zusätzlichen Risiken, die durch das Monitoring auftreten können, informiert.
Durch die Verwendung von „Korkenzieherelektroden“ konnte die Impedanz deutlich gesenkt werden. Hautverbrennungen durch die Nadelelektroden kommen daher bei spannungskonstanten Stimulationsgeneratoren nicht mehr vor. Verbrennungen können eher bei der Verwendung von monopolaren Kauterelektroden auftreten, daher ist auf den korrekten Sitz der Neutralelektrode zu achten. Es sollten sich keine Nadeln zwischen dem OPGebiet und der Neutralelektrode befinden. Durch transkranielle elektrische Stimulation können Krampfanfälle ausgelöst werden. Eine MEP-Stimulation bei Patienten mit bekanntem Krampfleiden ist daher kontraindiziert. Durch Verwendung von zu hohen Stromstärken können durch elektrische Stimulation beim anästhesierten Patienten Muskelschäden ausgelöst werden.
Durch die verwendeten Klicksignale mit einer Lautstärke bis 100 dB können AEP- Stimulationen den Hörapparat schädigen.
3. Ergebnisse
Ableitung elektrophysiologischer Potenziale
Bei nahezu allen Eingriffen traten Veränderungen in den Ableitungen auf, die das operative Vorgehen beeinflussten. Insgesamt ergab sich bei 89 Operationen (OP) ein richtig negatives Ergebnis. Dies bedeutet dass durch das Monitoring keine Schädigung der abgeleiteten Areale angezeigt wurde und der Patient postoperativ kein neurologisches Defizit zeigte. 14 Operationen führten zu einem richtig positiven Ergebnis, das heißt, intraoperativ kam es im IOM zu Veränderungen. Diese wiesen auf eine Verschlechterung der neurologischen Funktion hin. So hatte der Patient postoperativ zum Beispiel eine neu aufgetretene Lähmung oder Sensibilitätsstörung einer Extremität. Bei allen richtig-positiven Ergebnissen waren intraoperativ bereits Befunde erkennbar, die das operative Vorgehen beeinflusst haben. Trotzdem trat postoperativ ein neurologisches Defizit auf, das sich zum Teil wieder zurückbildete oder es entwickelte sich ein permanentes Defizit.
Insgesamt wurden nur zwei falsch positive Ergebnisse erhoben. So zeigte das IOM bei der Operation eine mögliche neurologische Verschlechterung an, wobei die betreffenden Patienten postoperativ kein neues neurologisches Defizit aufwiesen. Hierbei handelte es sich um eine Operation an einem Vestibularisschwannom und eine Operation bei einem Hirnstamm-Kavernom in sitzender Lagerung, bei der auch jeweils MEP-Ableitungen erfolgten. Im Verlauf der Operationen nahmen die MEP kontinuierlich ab und waren schließlich nicht mehr darstellbar. Postoperativ fand sich bei beiden Patienten kein neu aufgetretenes sensomotorisches Defizit. Im postoperativen kranialen Computertomogramm zeigte sich eine intrakranielle Luftansammlung. Diese muss zur Isolation des transkraniell elektrisch applizierten Reizes geführt haben. Bei keiner Messung trat ein falsch negatives Ergebnis auf. Folglich kam es bei allen Patienten, bei denen ein unauffälliges IOM durchgeführt wurde, auch postoperativ zu keinen neurologischen Ausfallerscheinungen.
Die Thenar-Muskulatur für die oberen Extremitäten und der M. tibialis anterior für die unteren Extremitäten zeigten die stabilsten und stärksten MEPAbleitungen. Bei insgesamt 15 von 105 Eingriffen veränderten sich die MEP. Bei drei von 15 Eingriffen verbesserten sich die MEP bereits während der Operation (Abb 7). Bei zwei von 15 Patienten waren die MEP postoperativ erloschen, ohne dass ein neurologisches Defizit auftrat. Bei zwei von 15 Patienten waren die MEP erloschen und es entwickelte sich postoperativ ein neues motorisches Defizit. Insgesamt 13 von 15 Patienten wiesen zwar eine Abschwächung/Änderung der MEP jedoch kein neurologisches Defizit nach dem Eingriff auf.
Die Abbildung 7 zeigt eine MEP-Ableitung einer Patientin, die an einem intraspinalen Meningeom in Höhe des Brustwirbelkörpers (BWK) 7/8 operiert wurde. Die Patientin hatte präoperativ eine inkomplette Querschnittssymptomatik und war nur wenige Schritte am Rollator gehfähig. Im Liegen wurde eine Parese der unteren Extremitäten vom Kraftgrad 3/5 nach MRC (Medical Research Council Schema) diagnostiziert. Die MEP-Ableitungen waren zu Beginn der OP nicht oder kaum erhältlich. Ungefähr 40 Minuten nach Beginn der Tumorverkleinerung beziehungsweise nach der Tumorentfernung erholten sich bereits intraoperativ die MEP. Der neurologische Status der Patientin besserte sich bereits am ersten postoperativen Tag deutlich. Die Hüftbeugung, Kniestreckung und Fußhebung stiegen auf den Kraftgrad 4/5. 10 Tage nach der OP konnte die Patientin auch ohne Rollator wenige Schritte gehen.
Die Abbildung 8 zeigt den Verlauf von MEP im M. tibialis anterior links bei einer Aufrichtung während einer Skolioseoperation. Es handelt sich hierbei um eine 15-jährige Patientin mit einer rechts konvexen Skoliose. Nach Aufrichtung verschlechterten sich die MEP auf der konkaven Seite deutlich. Innerhalb von 15 Minuten erholte sich das Potenzial jedoch. Die SEP wiesen eine dezente Verminderung der Amplitude bei erhaltener Latenz auf. Daher musste der Aufrichtungswinkels nicht erhöht werden. Der postoperative neurologischen Status der Patientin war unauffällig.
Bei einem 13-jährigen Jungen mit einem intraduralen, extraspinalen Ependymom wurde zu Beginn der Operation eine volatile Anästhesie (Sevofluran) durchgeführt. Hierunter kam es zu einer deutlichen Reduktion der Amplitude und Verzögerung der Latenz der evozierten Potenziale. Etwa 30 Minuten nach Umstellung auf eine TIVA (Propofol und Sufentanil) waren die Potenziale erheblich besser ableitbar (Abb 6) [2].
D-Wellen-Ableitung
In den insgesamt sechs Anwendungen der D-Wellen-Ableitung war bei einer Patientin das Vorschieben des Katheters in den spinalen Epiduralraum wegen narbiger Adhäsionen nicht möglich. In einem weiteren Fall traten während des Eingriffes unter der transkraniellen elektrischen Stimulation Herzrhythmusstörungen auf. In den übrigen Fällen, in denen die Methode problemlos anwendbar war, blieben die DWellen bis zum Ende der OP unverändert und ein neurologisches Defizit trat nach keiner dieser Operationen auf.
Während der sechs Operationen an intraspinalen, intramedullären Tumoren kam es bei drei Patienten zu Veränderungen der Tibialis-SEP. Eine Patientin zeigte nach einer Operation eines in - tramedullären Ependymoms einen inkompletten sensomotorischen Querschnitt. Bei dieser Operation waren die SEP intraoperativ erloschen. Die anderen zwei Patienten wiesen postoperativ keine neuen neurologischen Defizite trotz Veränderungen in den SEP auf.
Bei einer von insgesamt neun mikrovaskulären Dekompressionen des N. trigeminus verschlechterten sich die AEP, das heißt, hier verzögerte sich die Latenz der Welle V und die Amplitude war vermindert. Durch Korrektur der Spatellage erholte sich das Potenzial nach kurzer Zeit auf den Ausgangswert. Nach keiner mikrovaskulären Hirnnerven-Dekompression verschlechterte sich das Hören der kontralateralen Seite. Bei 13 Resektionen eines Akustikusneurinoms kam es in acht Fällen zu einem Ausfall des AEP auf der operierten Seite. Postoperativ trat in allen diesen Fällen eine Anakusis auf der entsprechenden Seite auf. Der intraoperative Verlust der AEP war hier mit großer Sicherheit mit einem postoperativen Hörverlust vereinbar.
Bei einer Resektion eines symptomatischen Kavernoms im Hirnstamm wurden ebenfalls AEP abgeleitet. Hier zeigten sich die ipsilateralen AEP am Ende der OP deutlich gemindert. Postoperativ erschienen beim Patienten keine neuen neurologischen Defizite. Eine bereits durch die Blutung bestehende Hypakusis, Facialisparese und Abducensparese bestanden direkt postoperativ weiterhin und erholten sich sogar bis zum Zeitpunkt der ersten Verlaufskontrolle nach drei Monaten. Wie es für alle evozierten Potenziale typisch ist, zeigte sich trotz Abschwächung der AEP intraoperativ eine Erholungstendenz bei entsprechender Anpassung der Operationstechnik.
Elektromyographie
Bei der Operation von Akustikusneurinomen treten regelmäßig EMG-Veränderungen am M. facialis auf. Die anschließenden Schweregrade der Ausfälle sind erwartungsgemäß sehr unterschiedlich. Bei insgesamt 61 Eingriffen stellten wir Veränderungen in den EMG fest. Vor allem bei Operationen mit Manipulation an Hirnnerven erfolgte hierdurch immer eine Anpassung des Ablaufes der Operation.
Bei einer Patientin entwickelte sich nach einem Polytrauma durch einen Sprengstoffanschlag mit Splitterverletzung unter anderem eine inkomplette traumatische N. radialis-Lähmung. Intraoperativ konnten anhand von EMGAbleitungen in der N. radialis-versorgten Muskulatur erhaltene und zerstörte Nervenanteile von einander abgegrenzt werden. Anschließend erhielt die Patientin eine Transplantation eines N. suralis-Interponats unter Aussparung der intakten Nervenanteile. Postoperativ trat kein neues neurologisches Defizit auf. Die neuralgiformen Schmerzen waren gebessert. Motorisch blieb eine inkomplette N. radialis-Lähmung unverändert.
Die Veränderung der abgeleiteten Potenziale zog gewöhnlich eine Änderung des Operationsablaufes nach sich. Wenn man die einzelnen Veränderungen näher betrachtet, so wurde die bipolare Koagulation in der Nähe von eloquenten Arealen eher gemieden. Vor allem bei Operationen an Akustikusneurinomen sind auch die vorübergehenden postoperativen Faciaisparesen in unserer Klinik dadurch seltener geworden. Die Lage der Spatel, eingebrachter Hirnwatten oder anderer Fremdkörper werden kontrolliert und gegebenenfalls korrigiert. Eine Änderung des Zugangsweges beziehungsweise der Präparationsrichtung kann auch dazu beitragen, evozierte Potenziale zu verbessern. Auf die Gabe von lokalen Vasodilatatoren wie Papaverin oder Nimodipin wurde bisher verzichtet.
Von den oben genannten relevanten Risiken des intraoperativen Monitorings zeigten sich in unserer Abteilung bei einer 77-jährigen Patientin mit einem intraspinalen, intraduralen Meningeom in Höhe des Brustwirbelkörpers 9 bei der Stimulation zur Ableitung von D-Wellen distal des OP-Gebiets Herzrhythmusstörungen mit Extrasystolen. Die D-Wellen-Ableitung wurde daher ausgesetzt. Die Rhythmusstörungen traten nicht mehr auf. Die Patientin zeigte postoperativ keine kardiologischen Defizite. Weitere durch das Monitoring ausgelöste Komplikationen kamen in allen anderen Operationen nicht vor. Insbesondere kam es nicht zu intraoperativen Krampfanfällen bei MEP, Hörminderung auf der kontralateralen Seite bei AEP oder zu Verbrennungen an der Einstichstelle der Stimulationselektroden.
4. Diskussion
Regelrechte Amplituden und Latenzen der intraoperativ abgeleiteten evozierten Potenziale sprechen für die funktionelle Integrität der beteiligten Axone. Nimmt die Amplitude ab oder ist das evozierte Potenzial nicht mehr ableitbar, ist ein Leitungsblock der betroffenen Axone eingetreten. Ein solcher Leitungsblock muss nicht notwendigerweise eine strukturelle Ursache haben. Ob eine strukturelle Ursache vorliegt und damit einen möglicherweise irreversiblen Funktionsverlust anzeigt, hängt von der Art und Dauer sowie dem Ausmaß der Schädigung ab.
Mit dem kontinuierlichen EMG ist eine permanente Überwachung eines motorischen Nervs oder eines Nervenanteils möglich. Veränderungen im EMG sind mit Schädigungen an diesen Strukturen vereinbar und sollten zu einer Änderung des Operationsablaufes am betroffenen Nerven führen. Durch die Ergänzung mittels evozierter Potenziale (MEP, AEP, SEP) ist eine noch genauere Überwachung möglich. Das zusätzliche Ableiten von MEP und schließlich von D-Wellen zeigt eine hohe Korrelation mit dem postoperativen Out-come (4, 5). Selbst bei vollständig fehlenden MEP und erhaltener D-Welle von 50 % der Ausgangsamplitude ist mit einer kompletten Erholung der neurologischen Funktion distal der operierten Höhe zu rechnen [6]. Das reine Ableiten von SEP während spinaler Eingriffe zeigte verständlicherweise eine eingeschränkte Aussagekraft über das eventuelle postoperative motorische Defizit [4].
Die Störungen in den SEP bei intramedullären Tumoren sind am häufigsten durch den dorsalen Zugang und damit durch eine Schädigung der Hinterstränge bedingt und lassen sich häufig nicht vermeiden. Trotzdem gehen sie nicht immer mit einer postoperativen Verschlechterung des neurologischen Status einher [7].
SEP-Ableitungen zeigen bei Operationen am Hirnstamm oder bei Gefäßeingriffen (Aneurysmaclipping, Carotis- Thrombendarteriektomie bei denen die Durchblutung von Hirngewebe eingeschränkt sein kann, einen hohen Stellenwert und sind gut mit dem postoperativen Out-come korreliert [8].
Klassischerweise wurde bei Skolioseoperationen ein intraoperativer Aufwachversuch mit neurologischer Funktionstestung bei dem Patienten unternommen. Unter einem IOM ist der Aufwachversuch nicht mehr notwendig. Eine eventuelle neurologische Verschlechterung kann direkt erkannt werden. Vor Entwicklung der MEP war es üblich, diese Operationen anhand von SEP, die jedoch lediglich die Hinterstrangfunktionen abbilden können, elektrophysiologisch zu überwachen. Durch den Einsatz von MEP lassen sich nun auch die motorischen Bahnen überwachen. Eine Verschlechterung der MEP führt zunächst nicht zwangsläufig zu einem neurologischen Defizit. Erst bei einem dauerhaften intraoperativen Verlust ist auch postoperativ mit einem bleibenden Schaden zu rechnen [3]. Nach der Aufrichtung bei einer Skolioseoperation können sich die MEP zumindest phasenweise verschlechtern (4, 5). Sinnvoll ist es, zunächst eine gewisse Zeit abzuwarten. Im oben genannten Fall erholten sich die Potenziale spontan nach circa 15 Minuten. Sollten sich die Potenziale nicht bessern, sollte eine Reduktion des Aufrichtungswinkels in Erwägung gezogen werden. Die SEP zeigten bei diesem Eingriff lediglich eine dezente Verminderung der Amplitude bei erhaltener Latenz. Ob sich die SEP bei einer relevanten Schädigung zusätzlich auch verändert hätten, ist ungewiss. Durch den Einsatz von IOM zur Ableitung von EMG-Potenzialen des N. facialis konnten die postoperativen Lähmungen der Gesichtsmuskulatur als direktes Ergebnis der Schädigung des N. facialis reduziert werden (9). Das „National Institute of Health“ verfasste bereits 1991 zum Thema „Acoustic Neuroma“ ein „Consensus statement“ in dem festgestellt wird, dass intraoperatives Echtzeit-Neuromonitoring das intraoperative Vorgehen bei Akustikusneurinomen verändert und darüber das postoperative Ergebnis verbessert [8].
Bei vaskulären Dekompressionen am Hirnstamm, Raumforderungen im Hirnstamm oder bei Operationen im Kleinhirnbrückenwinkel werden regelmäßig AEP abgeleitet [8]. Die Verwendung von IOM zur Vermeidung einer Ischämie durch den Spateldruck auf den Hirnstamm wird dringend empfohlen.
Durch den Einsatz von volatilen Anästhetika, zum Beispiel Desfluran oder Sevofluran, kommt es zu einer deutlichen Reduktion der Amplitude und Verzögerung der Latenz der evozierten Potenziale. Etwa 30 Minuten nach Umstellung auf eine TIVA, zum Beispiel Propofol und Sufentanil, verbessern sich die Potenziale erheblich [2]. Nach Relaxierung ist das Ableiten von EMG und MEP nicht mehr möglich. Bei isolierter D-Wellen-Ableitung hingegen wäre eine Relaxierung möglich, da lediglich oberoder unterhalb des OP-Gebietes stimuliert beziehungsweise abgeleitet wird. Da bei den Operationen in unserer Abteilung parallel zu den D-Wellen auch MEP abgeleitet wurden, waren alle unsere Patienten nicht relaxiert.
Durch den Einsatz von IOM kann in einer großen Anzahl von Operationen ein neurologisches Defizit verhindert werden. Die Lebensqualität der Patienten und ihrer versorgenden Angehörigen wird erhöht und die Dauer des Krankenhausaufenthaltes verkürzt sich. Die Kosten für das Gesundheitswesen werden damit verringert [9]. Nach einer Studie aus den USA können durch dieses elektrophysiologische Monitoring intraoperative Komplikationen verhindert und damit bei einer angenommenen Eintrittswahrscheinlichkeit von 2 % circa 1 000 000 Dollar pro 1 000 Patienten eingespart werden [10].
Seit über einem Jahr ist das IOM nun auch in Deutschland über die DRG abzurechnen. In der Folge nahmen zum einen die Häufigkeit der Anwender zu, zum anderen werden vermehrt medizinisch- technische Assistenten (MTA) eingesetzt, um das IOM anzulegen und zu überwachen.
Bisher existierten keine Ausbildungsmöglichkeit oder eine offizielle Anlaufstelle für Fragen und Schwierigkeiten um das IOM. Mit dem Ziel, eine einheitliche Ausbildung und eine wissenschaftliche Gemeinschaft zu schaffen, wurde 2007 die ISIN (International Society of Intraoperative Neurophysiology) gegründet. Sie ist neben einer nordamerikanischen Gesellschaft weltweit die einzige ihrer Art und bietet vor den zweijährigen Versammlungen einen „Hands-on Workshop“ zum Erlernen eines gewissen, international vergleichbaren, technischen Standards an. Erkrankungen wie Tumoren des zentralen oder peripheren Nervensystems sind in der Population der Bundeswehrangehörigen zwar selten vertreten, können dann aber für die operative Versorgung dennoch ein intraoperatives Monitoring erfordern [11].
Mit steigender Anzahl der verletzter Soldaten im Auslandseinsatz wird sich die Zahl der notwendigen neurochirurgischen Operationen erhöhen, nicht nur primär sondern auch sekundär und tertiär unter rekonstruktivem Aspekt [12]. Im weiteren Behandlungsverlauf kann daher auch der Bedarf an intraoperativer Überwachung zum Erhalt der neurologischen Funktion bei entsprechenden Verletzungsmustern notwendig sein. Gerade bei Schuss- oder Explosionstraumen treten vermehrt Verletzungen des Nervensystems auf.
Im Einsatz ist das elektrophysiologische Monitoring nicht relevant und für die allermeisten neurotraumatologischen Primärsituationen auch nicht erforderlich. Schon der erhöhte Zeit-, Materialund Personalaufwand zur Installation und Überwachung macht IOM im Einsatzszenario fragwürdig. Nach Verlegung zur weiterführenden Versorgung kann und sollte IOM bei bestimmten Operationen aber empfohlen und gegebenenfalls auch angewendet werden. Bisher wurden zwei Bundeswehrsoldaten und eine alliierte Regierungsbeamte im Behandlungsverlauf an traumatischen peripheren Nervenläsionen unter IOM operiert.
In vielen neurochirurgischen Kliniken ist es üblich, dass ein Assistenzarzt dazu bestimmt wird, das elektrophysiologische Monitoring durchzuführen. In manchen Abteilungen ist es hingegen üblich, dass Kollegen der Anästhesie oder auch Neurologie für das IOM verantwortlich sind. In wenigen größeren Kliniken existieren eigene Sektionen für Neurophysiologie, die das IOM sowohl in der klinischen Praxis als auch auf wissenschaftlichem Niveau betreiben. Die eigentliche Messung und Überwachung kann in die Hand einer erfahrenen MTA gelegt werden, die es allerdings bei der Bundeswehr in der STAN bisher nicht gibt.
5. Schlussfolgerungen
Wie auch in vielen weiteren klinischen Studien weltweit gezeigt wurde, sind bestimmte Veränderungen der evozierten Potenziale mit dem direkten postoperativen neurologischen Befund verknüpft. Durch den konsequenten Einsatz von intraoperativem elektrophysiologischem Monitoring können Bahnen im zentralen oder peripheren Nervensystem erhalten werden, wenn auf die Änderung der Potenziale auch eine Anpassung des operativen Vorgehens erfolgt. Mit zunehmender Anzahl an Verletzungen des zentralen oder peripheren Nervensystems wird auch der Bedarf der Bundeswehr an intraoperativem elektrophysiologischem Monitoring steigen.
Speziell für elektrophysiologisches Neuromonitoring vorgehaltene Personalstellen innerhalb der klinischen Fachabteilungen der Bundeswehrkrankenhäuser sind derzeit nicht existent. Daher wird das Monitoring auch in unserer Abteilung durch Assistenzärzte durchgeführt. Für die Zukunft wäre es wünschenswert, eine eigene MTA-Stelle für das IOM zu schaffen. Die Ausbildungsgrundlage müsste der MTA einer neurologischen Fachuntersuchungsstelle entsprechen. Eine Zusatzbezeichnung oder offizielle Ausbildungsverfahren für das intraoperative Monitoring existieren noch nicht.
Fotos: Abt. XII (Neurochirurgie) und XIII (Radiologie) BwKrhs Ulm
Danksagung:
Die Autoren danken Oberstarzt Dr. Danz für die Überlassung der MRT-Aufnahmen.
Interessenkonflikt:
Es besteht keine geschäftliche und keine andersartige Beziehung zwischen den Autoren und den Firmen der im Beitrag verwendeten Geräte und Hilfsmittel.
Literatur:
- 1 Cedzich C, Schramm J, Mengedoht CF, Fahlbusch R: Factors that limit the use of flash visual evoked potentials for surgical monitoring. Electroencephalogr Clin Neurophysiol 1988; 71: 142-145 .
- Sloan T, Rogers J: Differential effect of halothane on motor evoked potentials elicited by transcranial electric or magnetic stimulation in the monkey. J Clin Monit Comput 2009; 23: 163-168 .
- Owen J ., Bridwell KH, Grubb R et al.: The clinical application of neurogenic motor evoked potentials to monitor spinal cord function during surgery. Spine (Phila Pa 1976) 1991; 16: 385-390 .
- Nuwer MR, Dawson EG, Carlson LG, Kanim L E, Sherman JE: Somatosensory evoked potential spinal cord monitoring reduces neurologic deficits after scoliosis surgery: results of a large multicenter survey. Electroencephalogr Clin Neurophysiol 1995; 96: 6-11 .
- Kothbauer KF, Deletis V, Epstein FJ: Motor-evoked potential monitoring for intramedullary spinal cord tumor surgery: correlation of clinical and neurophysiological data in a series of 100 consecutive procedures. Neurosurg Focus 1998; 4: e1 .
- Kothbauer KF: Intraoperative neurophysiologic monitoring for intramedullary spinal-cord tumor surgery. Neurophysiol Clin 2007; 37: 407-414 .
- López JR: The use of evoked potentials in intraoperative neurophysiologic monitoring. Phys Med Rehabil Clin N Am 2004; 15: 63-84 .
- Consens Statement, Acoustic neuroma: Consensus statement / NIH Consensus Development Conference. National Institutes of Health Consensus Development Conference. 1991; 9: 1-24 .
- Wilson L, Lin E, Lalwani A: Cost-effectiveness of intraoperative facial nerve monitoring in middle ear or mastoid surgery. Laryngoscope 2003; 113: 1736-1745 .
- Deletis V, Shils JL: Neurophysiological monitoring during pedicle screw placement. In: Deletis V, Shils JL (eds): Neurophysiology in Neurosurgery: A Modern Intraoperative Approach. Amsterdam: Elsevier Science; 2002; 231-264 .
- Weber F, Knopf H: Incidental findings in magnetic resonance imaging of the brains of healthy young men. J Neurol Sci 2006; 240: 81-84.
- Mauer UM, Schulz C, Rothe R, Kunz U: German military neurosurgery at home and abroad. Neurosurg Focus 2010; 28: E14.
Datum: 31.08.2012
Quelle: Wehrmedizinische Monatsschrift 2012/5-6